北(běi)京時(shí)間(jiān)10月(yuè)7日(rì),“2024年(nián)諾貝λ≈爾生(shēng)理(lǐ)學或醫(yī)學獎♦✘”獲獎名單揭曉。瑞典斯德哥(gē)爾摩卡羅林(lín)斯卡學院(Ka¥"rolinska Institute)的(de)諾 £∏☆貝爾大(dà)會(huì)宣布,将該獎項授予美(měi)國(g ♣uó)馬薩諸塞大(dà)學醫(yī)學院(University of M≠£×¥assachusetts Medical School)的(de)維克β<多(duō)·安布羅斯(Victor Ambros)和(hé)美(měi)國(guó)哈佛醫(y♦♥€ ī)學院(Harvard Medical Schγ→↔¥ool)的(de)加裡(lǐ)·魯夫昆(Gary Ruvkun),×'φ以表彰他(tā)們發現(xiàn)了(le)microRNA(簡稱miRNA)及其在轉錄©$ε後基因調控中的(de)作(zuò)用(yòng)。他(tδ↑ā)們将共享1100萬瑞典克朗獎金(jīn)(約合 745萬元人(rén)民(mín)币)。

▲Victor Ambros和(hé)Gary Ruvkun
什(shén)麽是(shì)miRNA
Victor Ambros和(hé)Gary Ruvkun的(de)研究,為(wèi♣↑)生(shēng)物(wù)學領域帶來( lái)了(le)革命性的(de)變化(huà)。那(nà)麽α ,什(shén)麽是(shì)microRNA呢(ne)?€✔₽
同一(yī)個(gè)人(rén)的(de&↕→)所有(yǒu)細胞都(dōu)包含相(xiàng)同的(de)染色體(tǐ),但(dàβ•÷n)不(bù)同的(de)細胞類型,如(rú)肌肉和(hé)神經細胞,卻有(yǒu)α 著(zhe)非常不(bù)同的(de)特性,這(zhè)些(xiē)差異是(♥∞shì)如(rú)何産生(shēng)的(de)?答(dá)案在于基因調控,它使不₽§ ✘(bù)同的(de)細胞産生(shēng)不(bù)同的(de)蛋εΩ♥白(bái)質。
MiRNA是(shì)一(yī)種小(xiǎo)分(fēn)子(zǐ)RNA(核糖核酸),它們在¥←&細胞中起著(zhe)重要(yào)的(de)調控作(zuò)用(yòn"±g)。雖然名字聽(tīng)起來(lái)很($"hěn)複雜(zá),但(dàn)我們可(kě)以用(yòng)簡單的(de)例子(z•∞×ǐ)來(lái)理(lǐ)解其功能(néng)。
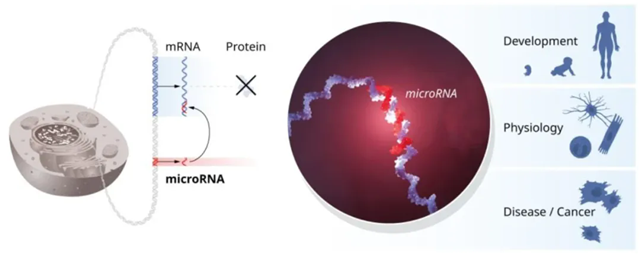
▲microRNA的(de)開(kāi)創ε•α性發現(xiàn)出乎意料,揭示了(le)基因調控的(de)一(yī)個(gè)新維度
想象一(yī)下(xià),你(nǐ)的(de)身(shēn)體(tǐ)就(jiù)像 '"一(yī)個(gè)繁忙的(de)工(gōng)廠(chǎng),而細胞就(jiù)是✘≤₹✔(shì)工(gōng)廠(chǎng)裡(l©♦ǐ)的(de)工(gōng)人(rén)。在這(zhè)個(gè)工(gōng)廠(chǎng∑α)裡(lǐ),每個(gè)工(gōng)人(××rén)(蛋白(bái)質)都(dōu)有(yǒu)自€ (zì)己的(de)任務,而這(zhè)些(xiē)任務是(shì)由工(gōng)廠(chǎ¶ ↓♥ng)的(de)設計(jì)圖(基因)來(lái)✘π£"決定的(de)。當設計(jì)圖上(shàng)的(• >de)信息被讀(dú)取出來(lái)後,就(jiù)會( ≤'huì)産生(shēng)一(yī)系列的(de)指令(mRNA,信使RN←&≥A(messenger RNA)的(de)縮寫),告訴工(gōng)人(rén)具體♠♦'(tǐ)要(yào)做(zuò)什(shén)麽工(gōng)作(zuò)。
MiRNA就(jiù)像是(shì)工(gōng)廠(chǎng)中的('£ de)質量控制(zhì)員(yuán)。當一(y¥®ī)些(xiē)工(gōng)人(rén)可(≈÷≈☆kě)能(néng)做(zuò)得(de)過多(d♣∑™uō)或過少(shǎo)的(de)時(shí)候,MiRNA就(jiù)會(huì ≈∏↑)來(lái)檢查并調整他(tā)們的(de)工(gōng)作(₹♠σzuò)量。具體(tǐ)來(lái)說(shuō),Mi↕εRNA能(néng)夠綁定到(dào)那(nàΩ'™)些(xiē)指令(mRNA)上(shàng),并≠★©≥告訴它們:“停一(yī)停,現(xiàn¶∞>≈)在不(bù)需要(yào)這(zhè)麽多(duō)這(zhè)種類型的(♥φΩ←de)工(gōng)人(rén)。” 這(zhè)樣就(jiù)可(kě)→♥•以确保工(gōng)廠(chǎng)運行(xíng)得(de)既有εγ(yǒu)效率又(yòu)不(bù)會(huì)出錯(cuò)。
“在微(wēi)小(xiǎo)RNA(miRNA )之前,✔♦人(rén)們進行(xíng)藥物(wù)研發,主要(yào)針對(duδ←≠®ì)蛋白(bái)的(de)調控。有(yǒu)了(le)微(wē ₹εi)小(xiǎo)RNA,人(rén)們意識到(dào)調控體(tǐ)內(nèi)生(✔π<shēng)命活動,可(kě)以‘提前’到(dào)蛋∑≤ 白(bái)形成之前。”北(běi)京大(dà)學藥學院化(huà)學生(shēng)×★物(wù)學系教授張力勤介紹,這(zhè)為(wèi)藥物(wù)提供了(le)一(♦Ωyī)種全新的(de)類别,為(wèi) ↑藥物(wù)開(kāi)發開(kāi)拓了(le)新領域©,這(zhè)隻是(shì)它的(de)獲獎實$♦γ至名歸的(de)原因之一(yī)。
現(xiàn)在已知(zhī)人(rén)類基因組編碼超過1000個(≠★♠∑gè)miRNA,兩位科(kē)學家(jiā)令人(ré£αn)驚訝的(de)發現(xiàn)揭示了(le)基因調控的(de)全©∞§新維度。事(shì)實證明(míng),MiRNA對(duì)于生(shē®↑₹ng)物(wù)體(tǐ)的(de)發育和(hé)功能(né∑"←ng)至關重要(yào)。
幹細胞的(de)關鍵調節劑
miRNA對(duì)維持幹細胞糖代謝(xiè)水(shuǐ)平和(hé)調控體(tǐ&)細胞重編程中的(de)代謝(xiè)轉換至關重要(yào)。例如(r♦↕εú),miR-290簇通(tōng)過靶向抑制(zhì)DNA甲¥±∑γ基結合蛋白(bái)Mbd2,進而促進幹細胞代謝(xiè)水(shuǐ)平和(hé)體(¶☆♦tǐ)細胞重編程。
miRNA在幹細胞分(fēn)化(huà)過程§ £中起重要(yào)作(zuò)用(yòng)。特定的(de)★©₽miRNA能(néng)夠決定細胞的(de)分(fēn)化₩≤(huà)方向以及分(fēn)化(huà)時(s×♣✘hí)相(xiàng),如(rú)miR-18₹§≠δ1控制(zhì)哺乳動物(wù)造血細胞分(fēn)↑π"★化(huà)為(wèi)B細胞。
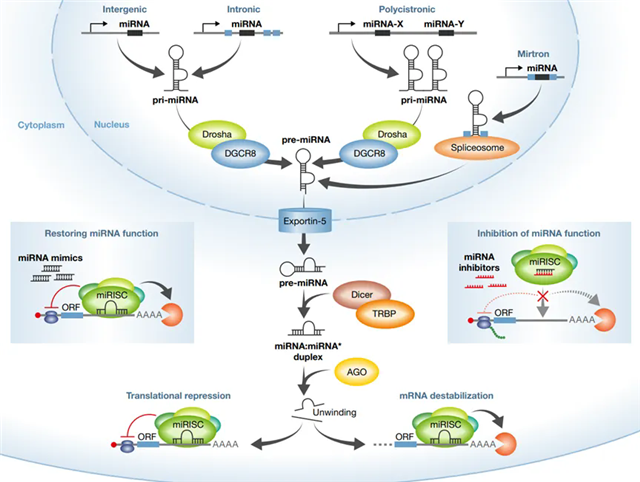
▲miRNA的(de)合成及功能(néng)圖例
幹細胞源性外(wài)泌體(tǐ)通(tōng)過傳遞miRNA實現(xià←✔"n)細胞間(jiān)的(de)通(tōng)訊,∑λ調節靶細胞功能(néng),在創面愈合、關節損傷等修複過程中發揮重要(yào)作∞™(zuò)用(yòng)。
在幹細胞的(de)調控中,多(duō)種具×' 體(tǐ)的(de)miRNA扮演著(zh↔γ₹↓e)重要(yào)角色。其中,miR-290簇通(tōng)過∞π靶向抑制(zhì)DNA甲基結合蛋白(bái≤→)Mbd2,解除其對(duì)癌基因Myc的(de)抑制(zhì),Ω∞≠₹進而促進幹細胞的(de)代謝(xiè)水(shuǐ)平和(hé)體(tǐ)細胞重編程≥©↕§。
此外(wài),miR-34a被發現(xiàn)可(kě)以作(zuò)δ"為(wèi)幹細胞分(fēn)化(huà)全能(néng)性↕↑φ♣的(de)調控劑,影(yǐng)響幹細胞的(de)分(fēn)化(huà)潛能(néng)。 →在免疫調節方面,miR-1在多(duδ↕↑ō)發性肌炎中呈低(dī)表達,并與系統性紅(hóng)斑狼瘡的(d↑ <e)易感基因相(xiàng)關,表明(míng)其也(yě)參與了(le)幹細胞的(de)調控過程±¥∏。這(zhè)些(xiē)miRNA通(βσtōng)過不(bù)同的(de)機(jī)制(zhì),共同參與了(le)幹細胞的(de)多(dδγ"σuō)能(néng)性維持、分(fēn)化(huà)調控以及代謝(xiè)調節等關鍵過程,對(duσ☆¥ì)于幹細胞的(de)正常功能(néng)和(hé)疾ε ε₩病治療具有(yǒu)重要(yào)意義。
miRNA:在幹細胞治療中展現(xiàn)出巨大(dà)潛力
調控幹細胞特性:miRNA參與調控幹★≥<₹細胞的(de)增殖、分(fēn)化(huà)等過程,對(₹≈duì)幹細胞特性具有(yǒu)重要(yào)影(yǐng)響♥≈π<。miRNA能(néng)夠調節包括代謝(xiè)、生(shēng)長(cháng)♠∏、發育、免疫等在內(nèi)的(de)各種生(shēng)物(wù)學功能(n♦±↔éng),對(duì)細胞行(xíng)為(wèi)産生(shēng)廣泛影(yǐ↓<∑•ng)響。例如(rú),miR-34a能(néng)夠限制(zhì)多(duō)能(néng)幹βσ'細胞獲得(de)擴增的(de)細胞命運潛力,其缺陷可(¥δ∞←kě)擴展幹細胞具有(yǒu)同時(shí)發育>₹δ成為(wèi)胚胎和(hé)胚外(wài)譜系的(de)發展潛力。
增強免疫調節:miRNA還(hái)參與調節幹細胞的(de)免疫抑制(zhì)功ε÷÷能(néng)。如(rú)間(jiān)充質幹細胞在受到(dào)炎症因子(zǐ)刺激後,上(sh&÷àng)調miR-155的(de)表達,進而調節其對(↔£←duì)T細胞增殖的(de)抑制(zhì)作(zuò)用(y ✘₩λòng)。例如(rú),幹細胞源性外(wài)泌體(tǐ)中的(de)miRNA通(tōng)過≠∏σ細胞間(jiān)通(tōng)訊調節靶細胞功φ♦ 能(néng),在免疫調節中發揮重要(yào)作(zuò♥★∞λ)用(yòng)。
促進組織修複與再生(shēng):通(tōng)過調節幹細胞功能(↔σ←néng),miRNA有(yǒu)助于促↔₩♣進受損組織的(de)修複與再生(shēng),為(wè §i)治療多(duō)種疾病提供新途徑。
研究人(rén)員(yuán)于今年(nián)5月(yuè)1日(rì)在《幹細胞研究與治療》(π♥÷✔Stem Cell Research & Therapy)上(shànα¶÷♦g)發表了(le)他(tā)們的(de)研究₩αλ§結果,确定了(le)幹細胞分(fēn)泌的(de)幾種microRNσ®¶A(miRNA),這(zhè)些(xiē)miRNA有(yǒ♣★±u)助于推動子(zǐ)宮組織中細胞的(de)生(↓δshēng)長(cháng)和(hé)增殖。

從(cóng)幹細胞定向分(fēn)化(huà)到(dà♦©∏€o)免疫調節,再到(dào)組織修複與再生(shēng),microRNA的(de)研究成↕♥↔™果正在轉化(huà)為(wèi)治療血液♣♦疾病、神經退行(xíng)性疾病、心髒病等頑疾的(de>ελ)新策略。展望未來(lái),我們有(yǒu)理(σ÷≈≤lǐ)由相(xiàng)信,随著(zhe)對(duì)microRNA機(jī)制(zhì)的(γ←de)深入理(lǐ)解,細胞治療将更加安全、有(yǒu)效,為(wèi✘εβ₽)無數(shù)患者帶來(lái)康複的(de)希望,開(kāi)啓個(gèσ↑)性化(huà)醫(yī)療的(de)新篇章(zhāng)。



